「経営計画2018」では、革新的な治療薬を生み出すための土台を構築

「変化する医療の最先端に立ち、科学の進歩を患者さんの価値に変える」。アステラスのVISION実現に向け、私たちはBreakthrough Science Developer(ブレークスルー サイエンス ディベロッパー)を目指しています。
ブレークスルー サイエンス ディベロッパーは、最先端の優れた科学技術やプラットフォームを探求し、それを様々な疾患や治療領域に活用することで、患者さんの新たな価値を創出していく企業のことです。
「経営計画2018」(「CSP2018」、対象期間:2018~2020年度)では、3つの戦略目標を掲げて取り組んできました。代表取締役社長 CEO*の安川健司は「CSP2018では、2020年代半ば以降の会社の屋台骨を支える革新的な治療薬を生み出すための土台を構築できた」と説明します。
以下、CSP2018における3つの戦略目標の進捗状況を紹介します。
*現代表取締役会長
戦略目標1:製品価値の最大化とOperational Excellenceの更なる追求
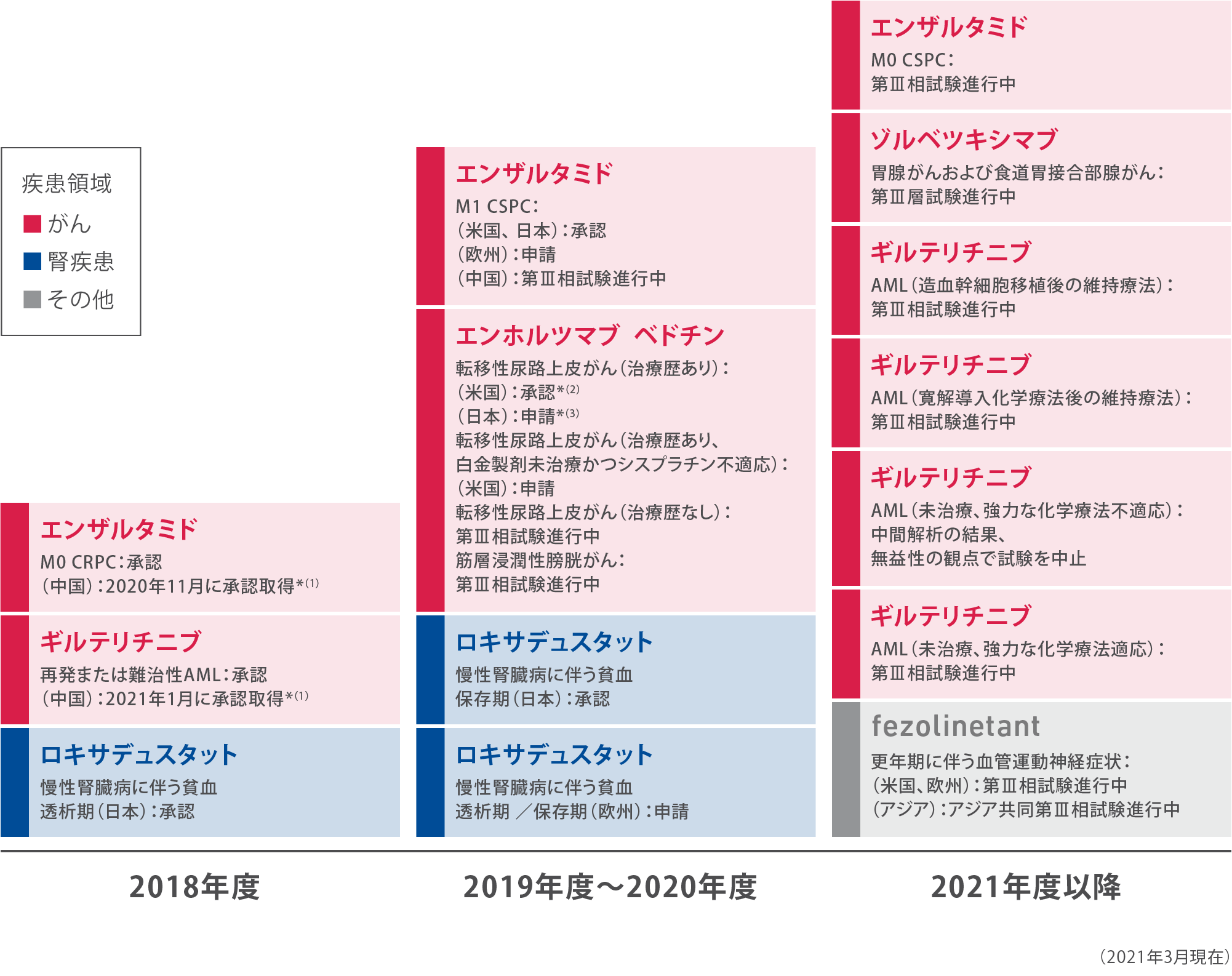
「6つの重点後期開発品(エンザルタミド、ギルテリチニブ、エンホルツマブ ベドチン、ゾルベツキシマブ、ロキサデュスタット、fezolinetant)の目指すマイルストンに向け、この3年間で着実に前進することができた」と安川は語ります。
CSP2018「今後の申請予定:重点後期開発品」のアップデート(現況と今後の予定)
M0 CRPC:非転移性去勢抵抗性前立腺がん, M1 CSPC:転移性去勢感受性前立腺がん, M0 CSPC:非転移性去勢感受性前立腺がん, AML:急性骨髄性白血病
*(1) CSP2018発表時に予定していなかった成果
*(2) 適応症:抗PD-1抗体薬または抗PD-L1抗体薬による治療歴があり、かつ術前または術後の補助化学療法として、あるいは局所進行または転移した状態において白金製剤による治療歴のある、局所進行性または転移性尿路上皮がん
*(3) 適応症:治療歴のある局所進行性または転移性尿路上皮がん
各重点後期開発品の進捗状況は、以下の通りです。
エンザルタミド(製品名:XTANDI®/イクスタンジ®)
前立腺がんは男性のがんの中で2番目に多く、全世界で年間約140万人が新たに診断されています*1。アステラスは、前立腺がんの治療薬としてエンザルタミドを世界各国で販売しています。
CSP2018 を発表した2018年5月の時点で承認を取得していたエンザルタミドの適応症は、転移性去勢抵抗性前立腺がん(M1 CRPC、日本での適応症は「去勢抵抗性前立腺癌」)でしたが、Pfizer Inc.と共同で、より早期の前立腺がんへの適応拡大ならびに更なる地域の拡大を目指し、この3年間開発を進めてきました。
その結果、非転移性去勢抵抗性前立腺がん(M0 CRPC)の追加適応について米国および欧州においてそれぞれ2018年7月および10月に承認を取得しました。また、転移性去勢感受性前立腺がん(M1 CSPC)の追加適応については、米国および日本においてそれぞれ2019年12月および2020年5月に承認を取得し、欧州では2019年7月にM1 CSPCについて承認申請し審査のプロセスが進行中です。一方で、中国では、2019年11月に転移性去勢抵抗性前立腺がん(M1 CRPC)の適応で承認を取得後、2020年3月より販売を開始し、さらに2020年11月にはM0 CRPCの追加適応についても承認を取得しました。アステラスは、グローバルでさらなる適応拡大を目指し開発を進めています。
*1 World Health Organization Globocan 2020
ギルテリチニブ(製品名:ゾスパタ®)
急性骨髄性白血病(AML)は高齢者が多く罹患するがんで、加齢とともに患者数が増加します。日本では約5,500人*2、米国では約19,000人*3、欧州では約18,400人*4がAMLと診断されています。AMLは生命に関わる疾患であり、できるだけ早期に治療を開始する必要があります。
CSP2018発表時点で、ギルテリチニブは成人の再発または難治性FLT3(FMS-like tyrosine kinase 3)遺伝子変異陽性AMLの治療薬として、日本および米国で承認申請の審査中でした。その後、日本、米国および欧州でそれぞれ2018年9月、11月および2019年10月に承認を取得し、販売しています。また中国では、2021年1月にFLT3遺伝子変異が確認された成人の再発または難治性のAMLに対する治療薬として、条件付き承認を取得しました。なお、より早期のAMLへの適応拡大を目指し、複数の臨床試験を実施中です。
*2 KantarHealth. TREATMENT ARCHITECTURE: JAPAN LEUKEMIA, ACUTE MYELOID. CancerMPact® Japan, February 2017
*3 American Cancer Society. Key Statistics for Acute Myeloid Leukemia (01-04-2018)
*4 Visser O, et al., 2012
エンホルツマブ ベドチン(製品名:PADCEV®)
尿路上皮がんは膀胱がんの90%を占めるがんです。全世界で年間約57万人が膀胱がんと診断され、約21万人が死亡しています*5。アステラスは、Seagen Inc. と共同でエンホルツマブ ベドチンの開発を進めており、局所進行性または転移性尿路上皮がん治療薬として米国で販売しています。
CSP2018発表時点で第II相試験*6が進行中でしたが、その試験結果に基づき、米国食品医薬品局(FDA)の迅速承認プログラムにより、2019年12月に米国で承認*7を取得し、同月に販売を開始しました。さらに、2021年2月に、米国で2つの生物学的製剤一部変更承認申請(sBLA)*8を提出しました。本sBLAの一つはPADCEVの迅速承認を正規承認へ変更することを目的としており、もう一つは適応拡大*9を目的としています。2021年3月には、日本で、治療歴のある局所進行性または転移性尿路上皮がんの適応について承認申請しました。また、中国においても臨床試験の準備を進めており、さらなる地域拡大を目指します。なお、より早期である未治療の転移性尿路上皮がん、ならびに筋層浸潤性膀胱がんについてもグローバルで臨床試験を実施しています。
*5 World Health Organization Globocan 2020
*6 第I相/第II相/第III相試験:臨床試験は、通常、第I相から第III相までの3段階で行われる。第I相は自由意思に基づき志願した健常成人を対象、第II相は比較的軽度な少数例の患者を対象、第III相は医薬品販売後に使用が見込まれる患者を対象とし、臨床試験が行われる。
*7 2019年12月に米国で迅速承認を取得した対象疾患:抗PD-1抗体薬または抗PD-L1抗体薬による治療歴があり、かつ術前または術後の補助化学療法として、あるいは局所進行または転移した状態において白金製剤による治療歴のある、局所進行性または転移性尿路上皮がん。
*8 生物製剤承認一部変更申請(sBLA:supplemental Biologic License Application):FDAに対する申請様式であり、生物製剤の適応症を追加する場合の申請方法。
*9 2021年2月に提出した適応拡大を目的としたsBLAの対象疾患:PD-1またはPD-L1阻害剤による治療歴があり、シスプラチン不適応の局所進行性または転移性尿路上皮がん。
ゾルベツキシマブ
胃がんは、全世界におけるがんによる死亡の原因として3番目に多いがんです*10。また、転移性胃腺がんおよび食道胃接合部腺がんでは5年生存率が20%に達しません*11。
CSP2018の発表時点で、ゾルベツキシマブは胃腺がんおよび食道胃接合部腺がんを対象に第III相試験を実施していました。3年が経過した2021年3月現在、上記の第III相試験に加えて膵臓腺がんを対象とした第II相試験も進行中です。なお膵臓がんは、がんによる死亡の原因として7番目に多く*10、5年生存率は4%*12と低いことで知られています。
*10 World Health Organization Globocan 2020
*11 Pennathur A, et al., 2013; Sahin et al., 2008
*12 Ilic M, et al., 2016
ロキサデュスタット(製品名:エベレンゾ®)
慢性腎臓病患者において、貧血は一般的にみられる合併症であり、透析期または保存期(透析導入前)の患者のいずれにおいても高い有病率と死亡リスクの増加が認められています*13。アステラスは、透析期および保存期の慢性腎臓病に伴う貧血を対象に、FibroGen, Inc. と共同で、日本、欧州、独立国家共同体(CIS)、中東、南アフリカ等においてロキサデュスタットの開発を進めています。
CSP2018の発表時点で、ロキサデュスタットは透析期および保存期の慢性腎臓病に伴う貧血を対象に、第III相試験を実施していました。その後、日本において、透析施行中の腎性貧血に対する適応について2019年9月に承認を取得し、同11月より販売を開始しました。保存期に対する適応追加については2020年11月に承認を取得しました。欧州では2020年4月に慢性腎臓病に伴う貧血を対象として承認申請をし、順調に審査のプロセスが進行しています。
*13 Stauffer ME, et al., 2014
fezolinetant
血管運動神経症状(顔のほてり・のぼせなど、ホットフラッシュ)(Vasomotor Symptoms:VMS)は閉経に伴ってしばしば見られる症状です。世界的に40~64歳の女性の50%以上で発症が報告されています*14,15。fezolinetantは、閉経に伴うVMSの頻度および重症度を軽減させるファーストインクラスの非ホルモン治療薬となる可能性があります。
CSP2018の発表時点で、fezolinetantは閉経に伴うVMSを有する患者を対象に、第II相試験を実施していました。その後、2019年8月から米国および欧州で3つの第III相試験を開始しており、そのうち2つの第III相試験ともに良好な結果が得られています。また、アジアでも2020年4月から第III相試験が進行中です。
*14 Utian WH. Psychosocial and socioeconomic burden of vasomotor symptoms in menopause: a comprehensive review. Health Qual Life Outcomes 2005; 3: 47
*15 Woods, NF, Mitchell ES. Symptoms during the perimenopause: prevalence, severity, trajectory, and significance in women’s lives. Am J Med. 2005;118(suppl 12B):14-24
戦略目標2:Focus Areaアプローチによる価値創造
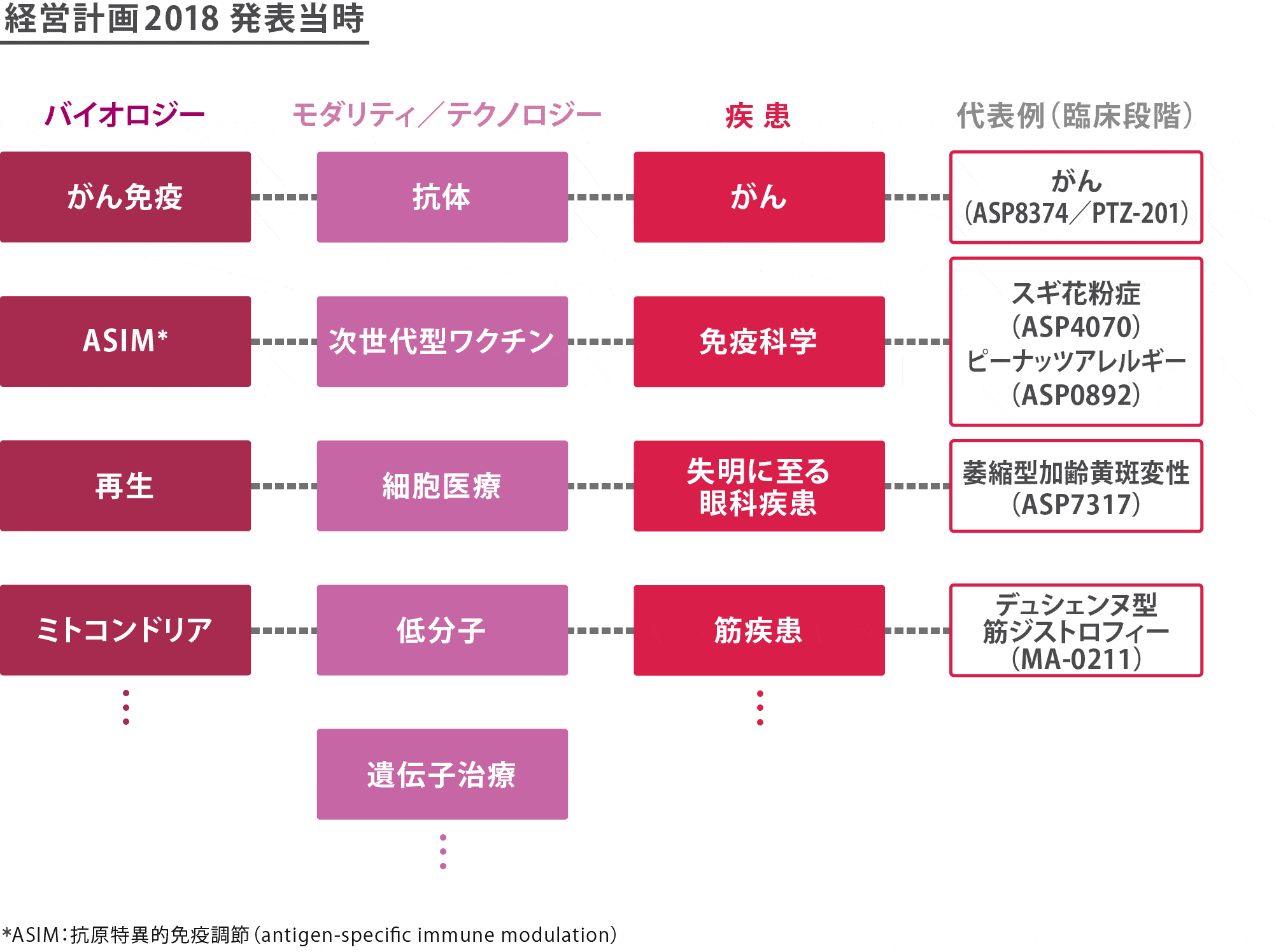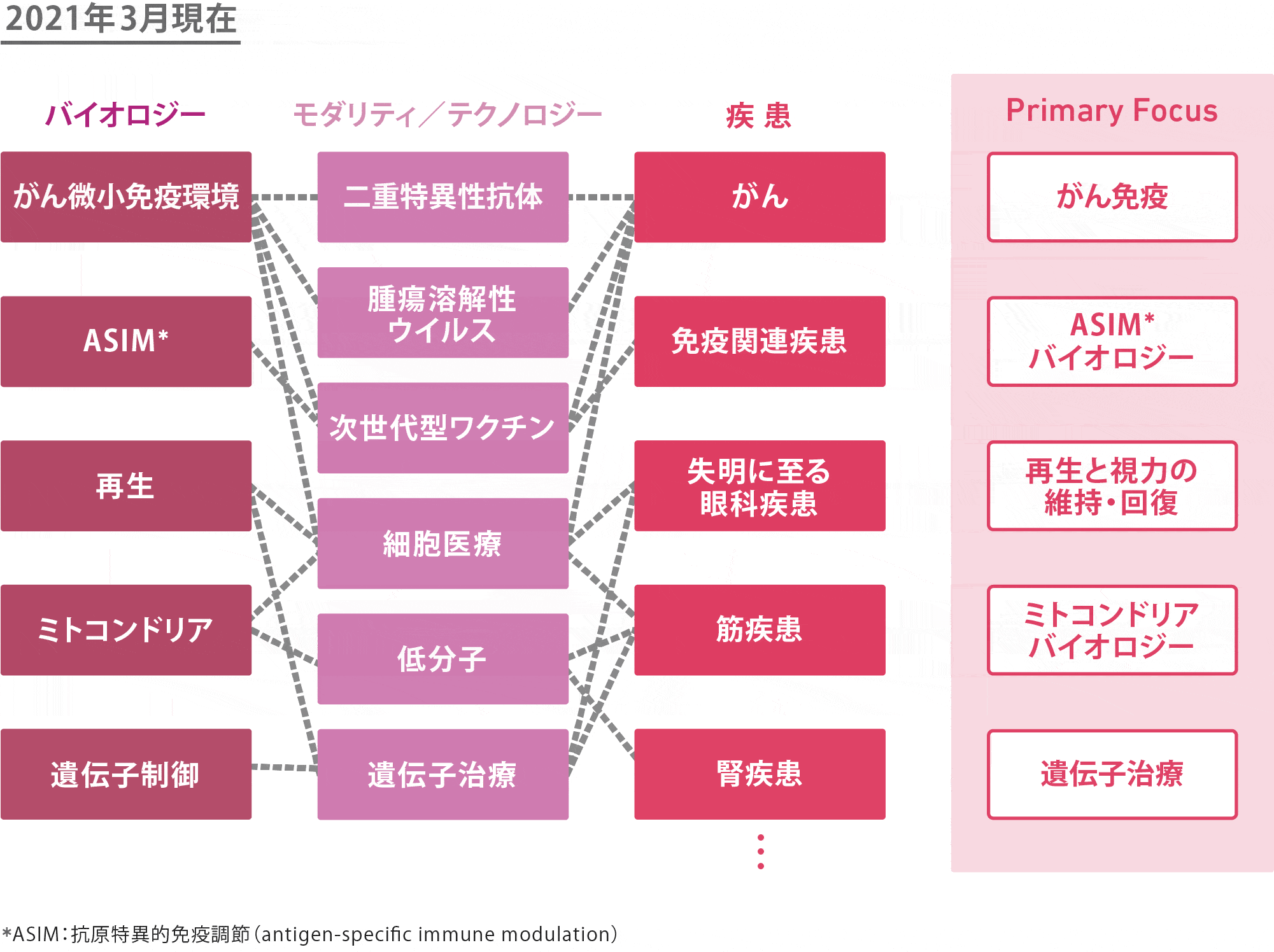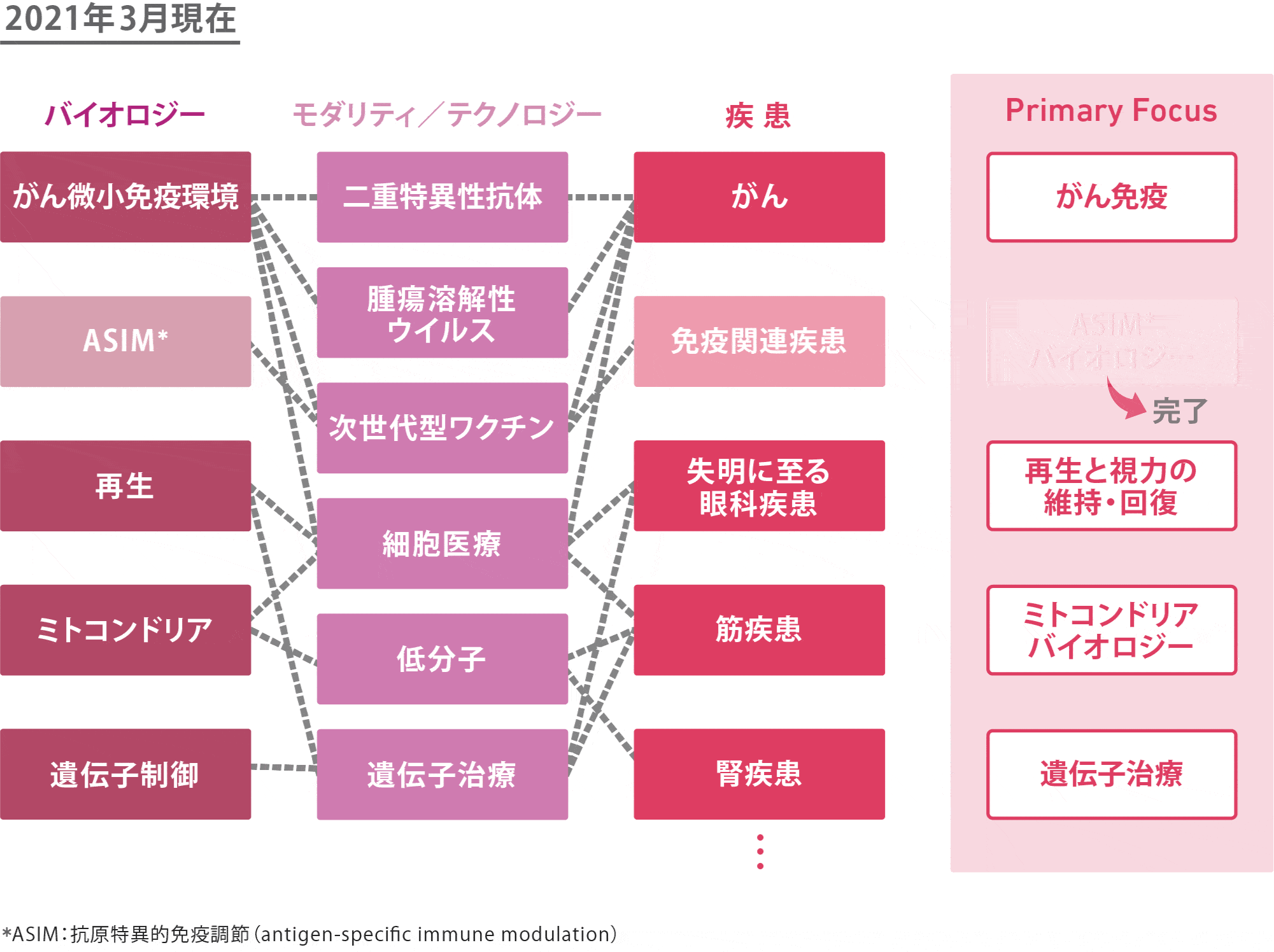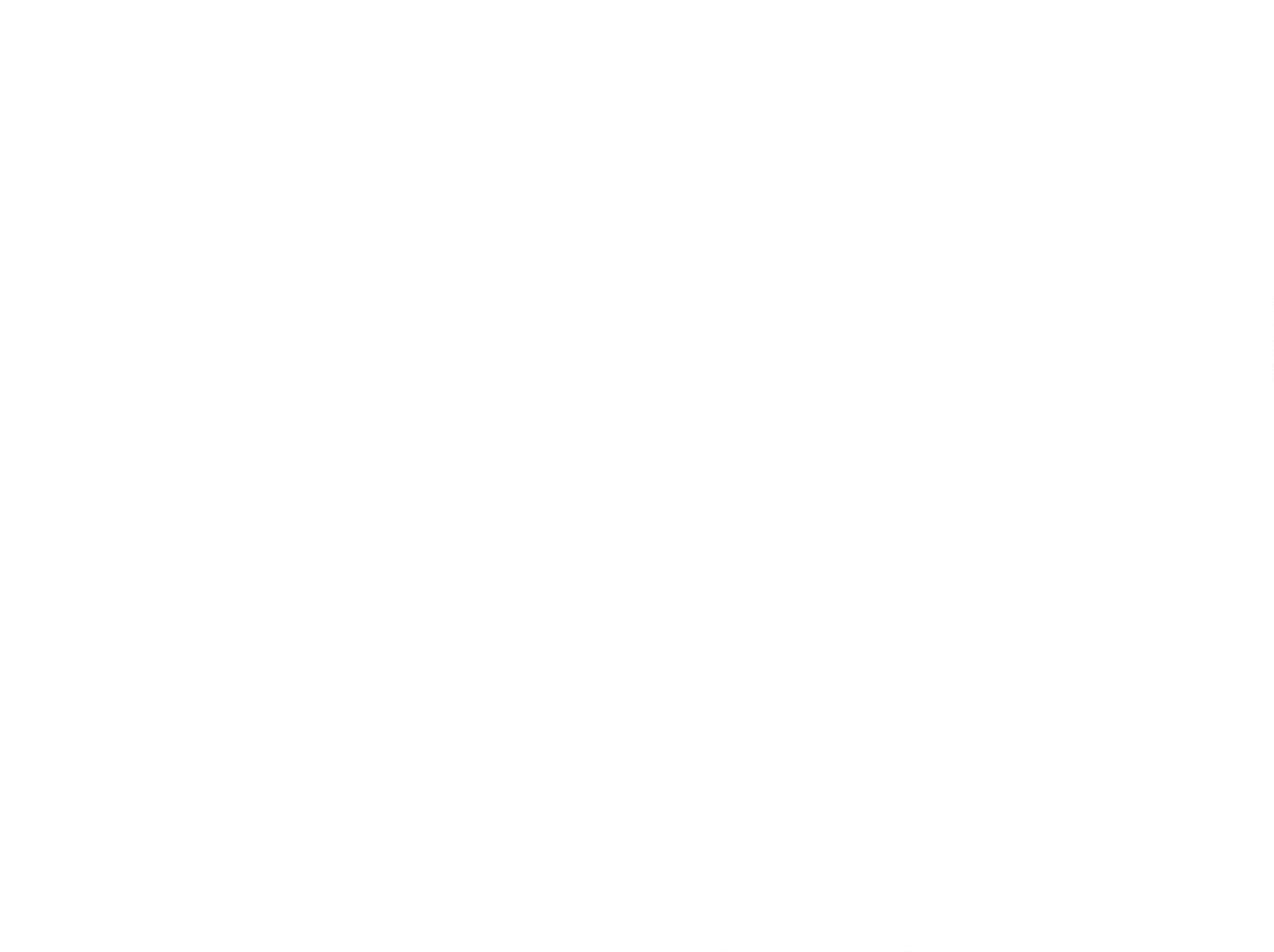
アステラスは2010年代半ばまで、泌尿器、がん、移植といった特定の疾患や治療領域において、革新的な医薬品を届けていくことで競争優位を確立するGlobal Category Leader(グローバル カテゴリー リーダー)モデルを展開していました。しかし、現在はターゲットとなる疾患を絞って薬を研究開発していくという従来の出口ありきの戦略から脱却し、多面的な視点で創薬ターゲットを絞り込むという新しいアプローチを取っています。それがFocus Area(フォーカスエリア)アプローチです。
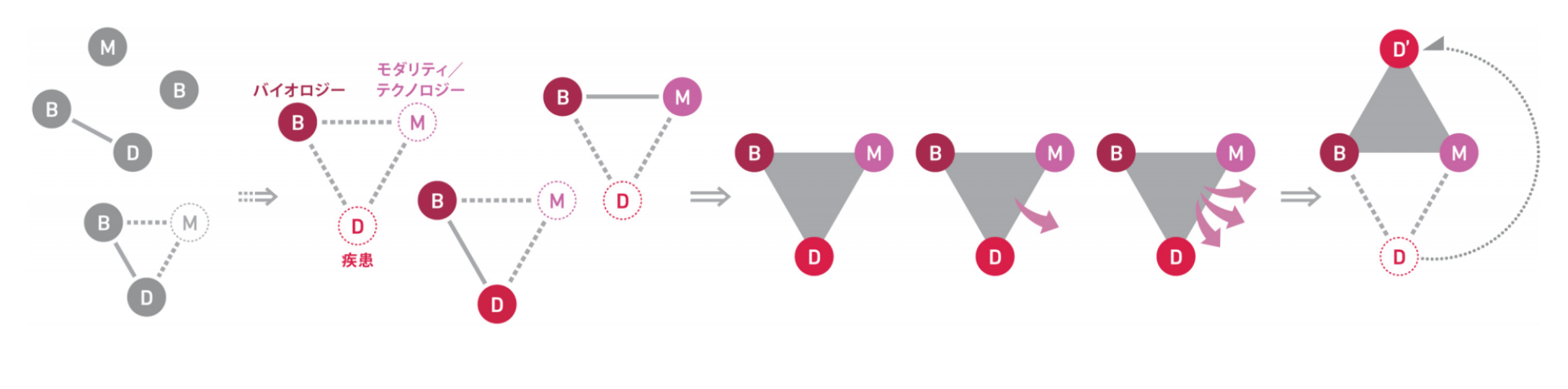
Focus Areaアプローチでは、3つの構成要素、(1)病態関連性が高いバイオロジー*16、(2)汎用性のあるモダリティ/テクノロジー*17、(3)これらバイオロジー、モダリティ/テクノロジーの2つの要素により解決が期待されるアンメットメディカルニーズ(いまだ満たされていない医療ニーズ)の高い疾患の組合せの集合をFocus Areaとして定義しています。
安川は「このバイオロジー、モダリティ/テクノロジー、疾患を頂点とする三角形がひとたび形成されると、プロジェクト創出が単発では終わらず、そこから芋づる式に新薬を生み出すことが出来る」と説明します。
複数の新薬候補が生み出され、リード化合物が臨床段階まで進んだ時に、Primary Focus(プライマリフォーカス)という、社内で最優先に経営資源を投下する領域として認定することにしました。
2018年の時点で、このアプローチはまだ模索段階にありましたが、これまでに5つがPrimary Focusとして認定され、その内の1つは複数のプログラムが臨床段階に進み、創薬研究が完了しました。現在は「再生と視力の維持・回復」、「ミトコンドリアバイオロジー」、「遺伝子治療」、「がん免疫」の4つをPrimary Focusとして認定し、それぞれ実績を積み上げています。
アステラスは、競争優位の源泉となる自社のコアケイパビリティ(専門能力)に磨きをかけるとともに、様々な社外の優れたケイパビリティを積極的に取り入れる提携やパートナーシップの機会を探索しています。ナンナ(Nanna)社、オーデンテス(Audentes)社、ザイフォス(Xyphos)社、ポテンザ(Potenza)社、ケセラ(Quethera)社、ユニバーサルセルズ(Universal Cells)社、マイトブリッジ(Mitobridge)社の買収はその一環です。
*16 バイオロジー:免疫科学やミトコンドリアの異常など疾患の原因となる仕組み。
*17 モダリティ/テクノロジー:低分子、抗体、遺伝子治療や細胞治療など治療コンセプトを実現するための治療手段・技術。
各Primary Focusの概要と進捗状況は、以下の通りです。
Primary Focus「再生と視力の維持・回復」
Primary Focus「再生と視力の維持・回復」は、失明の不安から患者さんを解放し、視力を取り戻す希望の光をもたらすことを使命にしています。細胞医療や遺伝子治療という次世代モダリティを活用することで、失明リスクの高い後眼部疾患を有する患者さんに対して、視力の維持や回復をもたらす新たな治療選択肢を提供します。これまで治療法が無かった患者さんに対して、一回の治療によって長期的な視力の維持・回復を達成することを目指しています。
地図状委縮を伴う加齢黄斑変性を対象とした細胞医療のプログラムであるASP7317については、現在第I相試験を実施中です。一般に、再生医療に用いられる細胞は、低分子化合物と異なり、製造や物流においても高度な品質管理が必要ですが、アステラスでは、商用レベルの細胞にて既に臨床試験を実施し、初期商用生産までカバーできる細胞製造プロセスが確立できています。
また高品質な細胞医療製品の安定供給に向け、米国ボストン近郊に、7つのクリーンルームを持つ工場を新設、2020年10月から稼働を開始し、研究から初期商用生産までを一気通貫で取り扱う体制も整っています。
本Primary Focusの詳細はこちらをご覧ください。
Primary Focus「ミトコンドリアバイオロジー」
Primary Focus「ミトコンドリアバイオロジー」のターゲットであるミトコンドリアの機能はとても複雑です。エネルギーを産生する細胞内小器官というのが最も一般的な理解ですが、ミトコンドリアにはそれ以外にも多面的な機能があり、それらは複数の生化学的な経路で制御されています。事実、ミトコンドリアは老化に関わるプロセスにおいて重要な役割を果たしており、ミトコンドリアの機能が異常をきたすと、様々な疾患の原因になったり、その症状を悪化させたりすることが知られています。
2018年に買収したマイトブリッジ社と共同で開発しているペルオキシソーム増殖因子活性化受容体デルタ(PPARδ)調節薬(ASP0367)が、原発性ミトコンドリアミオパチー治療薬としての開発について、FDAからファストトラック*18の指定を受けました。現在第II/III相試験の準備を進めています。また、他のPPARδ調節薬(ASP1128)においても冠動脈バイパス手術後の急性腎不全を適応としてFDAからファストトラックの指定を受けており、第II相試験を実施中です。
2020年4月にはナンナ社を買収しました。ナンナ社が持つ細胞内標的に作用する化合物のスクリーニングプラットフォームと、これまで私たちが培ってきたミトコンドリアバイオロジーのケイパビリティを組み合わせて、ミトコンドリア関連疾患に対する革新的な治療法の開発を進めています。
さらに、本Primary Focusのポートフォリオは低分子化合物で構成されていましたが、今後はそのモダリティを細胞医療にも拡げていく予定です。
本Primary Focusの詳細はこちらをご覧ください。
またPPARδ調節薬の詳細は「Primary Focusミトコンドリアバイオロジー ~第二章 プログラム~」をご覧ください。
*18 ファストトラック:米国における優先審査制度の一つで、アンメットメディカルニーズが高い重篤または生命を脅かす恐れのある疾患に対する治療薬の開発および審査が迅速化される。

Primary Focus「遺伝子治療」
遺伝子治療は医療に大きな変革をもたらす力を秘めています。遺伝子コードの突然変異または欠損は約7,000種類にも及ぶ遺伝性疾患*19の直接的な発症原因になっているだけではなく、遺伝性でない、その他多くの一般的な疾患の病態生理にも寄与しています。近年、安全な遺伝子導入・制御技術が急速に進歩し、実用化に至っています。遺伝子治療は、他に治療選択肢がない患者さんに革新的な価値をもたらす可能性を秘めています。
本Primary Focusでは、アデノ随伴ウイルス(AAV)をベクターとした遺伝子治療におけるグローバルリーダーを目指し、ケイパビリティの獲得を進めています。2020年1月、希少な神経筋疾患を対象とした遺伝子治療薬の開発をリードするオーデンテス社を買収し、同社の臨床での有効性が確認されたリードプログラム、大規模製造能力、AAV技術プラットフォームなどの卓越したケイパビリティを入手しました。現在 X連鎖性ミオチュブラーミオパチー(XLMTM)に対する遺伝子置換療法(AT132)、重篤な進行性神経筋疾患であるポンペ病に対する遺伝子置換療法(AT845)など、複数のプログラムの臨床試験が進行中です。
オーデンテス社が遺伝子治療のCenter of Excellence(CoE、中核拠点)となり、オーデンテス社が有するケイパビリティと、アステラスが持つグローバルスケールの事業体制およびリソースを融合させ、本Primary Focusのさらなる前進に向けて取り組んでいます。
本Primary Focusの詳細はこちらをご覧ください。
*19 Online Mendelian Inheritance in Man®(OMIM®)Gene Map Statistics. https://www.omim.org/statistics/geneMap,(参照2021年3月17日)

Primary Focus「がん免疫」
Primary Focus「がん免疫」における私たちの使命は、革新的ながん治療薬を研究開発し、そして患者さんに届け、最終的にはがんを治癒することです。この使命を達成するために、私たちはイノベーションを可能とする能力を高め、外部パートナーとの強力なネットワークを構築しています。免疫チェックポイント阻害剤のような新しい治療方法が登場しましたが、依然としてがん治療にはアンメットメディカルニーズが存在しています。免疫チェックポイント阻害薬を投与された患者さんの80%は治療に抵抗性であるか、治療中に再発すると推定されています。
本Primary Focusでは、がんに対する免疫応答の様々なステップへ同時に作用する治療薬の開発に取り組んでいます。また外部パートナーとの戦略的な提携により、競争力のあるがん免疫のポートフォリオを確立しています。現在、複数のプログラムが第I相段階にあります。ポテンザ社買収により獲得しアステラス単独で取り組んでいるプログラムには、抗NRP1(neuropilin-1)抗体(ASP1948)や、GITR(glucocorticoid-induced TNFR-related protein)アゴニスト抗体(ASP1951)があり、また外部パートナーと共同で取り組んでいるプログラムには、鳥取大学と実施中の腫瘍溶解性ウイルス(ASP9801)や、理化学研究所と実施中の人工アジュバントベクター細胞(aAVC)(ASP7517およびASP0739)があります。
本Primary Focusでは、さらなるパイプライン拡充に向けて、細胞医療を用いたがん免疫のプラットフォームを立ち上げました。また2020年からザイフォス社が、がん免疫におけるCoEとしての活動を開始しています。
本Primary Focusの詳細はこちらをご覧ください。
Primary Focusの有機的な繋がり
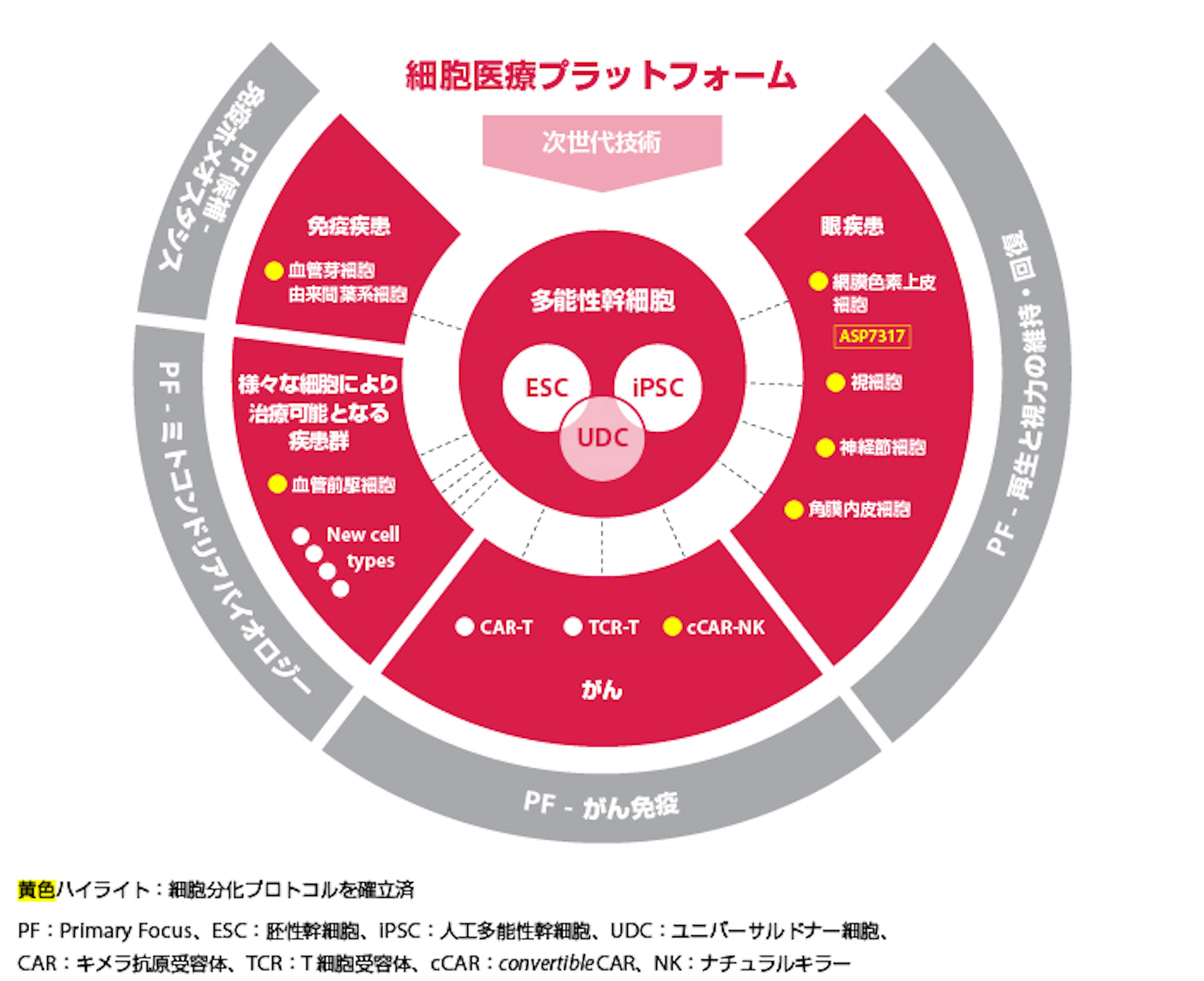
各Primary Focusの進捗に加え、もともと独立していたPrimary Focus同士が有機的に繋がり始めています。各Primary Focusで研究していたモダリティ/テクノロジーが、下図のように、他のPrimary Focusでも活用されることで、様々なバイオロジーや疾患への展開が進んでいます。
例えば、CSP2018発表時点では、主にPrimary Focus「再生と視力の維持・回復」にだけ活用されていた細胞医療プラットフォームが、「がん免疫」や「ミトコンドリアバイオロジー」など、複数のPrimary Focusにおいて有機的に活用されるようになり、この3年でパイプラインの充実化を達成しました。その中にはユニバーサルドナー細胞(UDC)技術*20を活用した次世代プロジェクトも含まれています。
現在、上図の通り、臨床試験中の網膜色素上皮細胞に続いて、その他の眼疾患、免疫疾患、がん領域のプロジェクトにおいて、臨床試験に向けた準備を進めています。特に、黄色で示している細胞は、既に分化プロトコルが確立された細胞で、今後GMP*21対応に向けた検討を進めていきます。
私たちは2025年までに、様々な疾患領域への展開に向けて細胞医療プラットフォームを発展させていきます。
細胞医療の詳細はこちらをご覧ください。
*20 ユニバーサルドナー細胞(UDC)技術:細胞への遺伝子導入ツールの一つである遺伝子組換えアデノ随伴ウイルス(rAAV)を用いた遺伝子編集技術に基づきヒト白血球型抗原(HLA)を改編することで、免疫拒絶反応を抑えた多能性幹細胞を作製する技術。
*21 GMP:Good Manufacturing Practiceの略。医薬品および医薬部外品の製造管理及び品質管理の基準。
戦略目標3:Rx+®プログラムへの挑戦
アステラスのVISION「変化する医療の最先端に立ち、科学の進歩を患者さんの価値に変える」を実現するために、これまで私たちが取り組んできている病気を治療する薬(医療用医薬品:Rx)の創製を通じて獲得した強みを活かしながら、Rxとは異なるアプローチで患者さんに価値を提供することができると考えました。こうした考え方に立ち、新たに取り組みを開始したのがRx+®事業の創出です。

2018年4月にRx+事業創成部を設立し、Rx+®事業創出の戦略的方向性を示す「Rx+ Story®」を定め、「科学的根拠に基づくヘルスケアソリューションによって、心身ともに健康に、自分らしく生きることができる社会」の実現を目指しています。Rx+ Story®実現に向けて注力する事業領域を「スフィア」と名付け、それぞれのスフィアにおいて事業創出活動に鋭意取り組んでいます。
スフィア「慢性疾患の重症化予防」においては、2020年9月に神奈川県で運動支援サービスFit-eNce®(フィットエンス)の提供を始めました。これは科学的根拠のある運動プログラムを継続的に実施することにより、2型糖尿病をはじめとする様々な疾患の治療に役立てる支援サービスです。これがRx+®として初めて軌道に乗せた事業となりました。
スフィア「デジタル×ニューロサイエンス」においては、画期的な極小の体内埋め込み型医療機器について共同研究を続けてきたiota社が、2020年10月にアステラスの仲間に加わりました。アステラスのバイオエレクトロニクスへの取り組みの基盤として、Rx+®事業を加速させていきます。
また、スフィア「手術・診断制度向上による患者アウトカム最大化」においては、腹部および骨盤内手術時に尿管を可視化する蛍光造影剤(ASP5354)で第II相試験での投与を開始しました。実際に尿管が可視化されることが、早くも臨床試験で確認できています。手術中に尿管を可視化する可能性のある新たなアプローチとして、米国FDAからはファストトラックの指定を受けました。
安川はRx+®事業の成果をこう振り返ります。「この3年間で、ヘルスケアイノベーションのポートフォリオを築き、強固な事業基盤を確立することが出来ました。今後も、Rx+ Story®をいち早く実現化するための体制を強化し、ビジネスをいつまでにどのように開始するのかという道筋や、経営への寄与の程度を明確にしながら、ゴールの実現に向けて進んでいきます」
Rx+®事業についての詳細はこちらをご覧ください。

新経営計画の発表に向けて
2021年5月に、2021年度から2025年度までの5カ年を対象とした新経営計画を正式に発表します。アステラスは製薬企業としての社会的使命を考え、常に環境の変化に適応しつつ先を見据えた行動をとる必要があり、新経営計画にもこうした取り組みを盛り込んでいきます。本「ストーリー」セクションにおいて新経営計画を特集する予定です。是非ご覧ください。
関連リンク